
- 分享收藏
胡瑾:功能医学专业分享|非肥胖型多囊卵巢综合征的功能医学辅助干预案例
简介

作者言:
据相关研究显示,多囊卵巢综合征(PCOS)发病率近年来呈上升趋势,目前发病机制尚未明确,该疾病涉及糖代谢、蛋白质、神经内分泌等多个方面异常情况,患者临床表现具有多种多样的特点,治疗方式难以统一。临床流行病学对病因进行调查,发现其发病因素与遗传、神经内分泌、心理因素、饮食及环境等具有密切相关性,应早期对发病相关因素进行分析,实施有效的措施,预防不良情况发生。
临床流行病学调查还显示 30% ~75%的 PCOS 患者存在超重或肥胖,另外有一部分患者属于非肥胖型(甚至是消瘦型)多囊卵巢综合征。今天分享案例为非肥胖型多囊(消瘦型)多囊卵巢综合征。
多囊卵巢综合征的简介:
多囊卵巢综合征(PCOS)于1935年被首次报道,主要表现为青春期少女和育龄妇女内分泌紊乱和代谢障碍综合征,可严重影响患者尤其是育龄期女性的生理、心理健康。在我国汉族19~45岁育龄妇女中的PCOS发病率为5-10% 。
PCOS典型的临床表现:月经稀发或闭经、不孕、多毛及卵巢多囊样改变,部分病人有痤疮及黑棘皮症。
PCOS典型内分泌特征:高雄激素血症、血浆LH水平增高、LH/FSH值增高(常常>2);且常常伴有显著的代谢异常:包括肥胖、高胰岛素血症、胰岛素抵抗、代谢综合征等。严重影响患者的生命质量、生育及远期健康。
诊断及诊断标准:
因临床表型的异质性,诊断标准存在争议。国际上先后制定 NIH、鹿特丹、AES 等多个诊断标准,目前采用较多的是鹿特丹标准;2018年《中国多囊卵巢综合征的诊疗指南》提出——月经稀发或闭经或不规则子宫出血是诊断必须条件。月经稀发或闭经的判断标准:初潮2~3年不能建立规律月经;闭经—停经时间超过3个以上;月经周期或≥6个月;月经稀发——即周期≥35天及每年≥3个月不排卵者。注意月经规律并不能作为判断有排卵的证据。
需要结合基础体温(BBT)、B超监测排卵、月经后半期孕酮测定等方法有助于判断是否有排卵)。另外,再符合下列2项中的一项,即可诊断为PCOS:
a) 高雄激素的临床表现或高雄激素血症。其临床表现如下:
-
痤疮:(复发性痤疮,常位于额、双颊、鼻及下颌等部位)。
-
多毛:(上唇、下颌、乳晕周围、下腹正中线等部位出现粗硬毛发)。
-
雄激素水平升高的生化指标:总睾酮、游离睾酮指数或游离睾酮高于实验室参考正常值。(需要注意在月经周期的第3~5天检查,包括睾酮、雌二醇、催乳素、LH和FSH。同时检查游离睾酮、雌酮和胰岛素水平。如果月经周期不规则,不能确定抽血时间的时候,先做一个B超,可在B超检查没有见到优势卵泡,也就是最大卵泡直径小于10mm的时候,抽血检查)。
b) 超声表现为卵巢多囊改变(PCO):超声提示一侧或双侧卵巢直径 2~9mm 的卵泡≥12 个,和(或)卵巢体积≥10ml。
其中PCO的检查——超声检查前应停用口服避孕药至少1个月,在月经规则患者中应选择在月经周期第3天~第5天检查;稀发排卵患者若有卵泡直径>10mm或有黄体出现,应在下个周期进行复查,无性生活者,可选择经直肠超声检查,其他患者选择经阴道超声检查。
具备上述PCOS诊断条件后还必须逐一排除其他可能引起高雄激素的疾病(先天性肾上腺皮质增生、库欣综合征、分泌雄激素的肿瘤等)和引起排卵异常的疾病(高泌乳素血症,卵巢早衰和垂体或下丘脑性闭经,甲状腺功能异常等)才能确定诊断。也就是说PCOS的诊断是排除性诊断。
按照多囊卵巢综合征的诊断标准,可以将PCOS分为:高雄合并排卵功能障碍、高雄合并卵巢多囊样改变、排卵障碍合并卵巢多囊样改变,以及三个诊断标准都存在的PCOS表型。
主要差别:月经不规律的情况、不孕率存在差异。传统上,认为较为严重的多囊卵巢综合征:既有高雄激素,又有卵巢多囊样改变和排卵功能障碍的患者,月经紊乱和不孕率的发生率均较高。育龄期PCOS患者的代谢综合征和胰岛素抵抗发病率类似。
PCOS内分泌和代谢特征
首先是PCOS代谢风险增加在育龄期主要引起生殖紊乱,主要影响经期紊乱、多毛、性激素紊乱、不孕;随着年龄增加,代谢紊乱的风险增加,妊娠并发症、生活质量下降、糖尿病、心血管疾病、癌症风险增加。
PCOS机体代谢异常引发多种疾病,影响长期生活质量。
总结起来,其代谢效应主要表现为高胰岛素血症、胰岛素抵抗、糖耐量受损、血脂异常,腹型肥胖,超重/肥胖,高血压、内皮功能紊乱、脂肪肝等。
有研究显示:1.引起PCOS代谢异常的通路包括(1) 糖酵解、脂解、蛋白水解、尿素合成途径被促进。(2) 三羧酸循环、生酮途径被抑制。
2.肥胖、卵巢多囊样改变、高雄激素血症、代谢综合征、高血压和高脂血症均随年龄增加而增加。
查阅PCOS相关文献发现,对肥胖型PCOS研究报道的比较多,但对非肥胖型PCOS研究报道比较少。有研究显示非肥胖的PCOS患者主要表现为下丘脑一垂体一卵巢轴(HPO轴)功能紊乱,患者具有更高的FSH、LH水平及LH/FSH,而不伴有IR的生化特征。主要引起月经紊乱,不排卵或稀发排卵,最终导致不孕,因此,非肥胖PCOS患者治疗应着重调整HPO轴的功能,恢复正常月经、有生育需求者帮助促排卵指导受孕。而肥胖的PCOS患者主要表为现胰岛素抵抗引起的高雄激素血症为主,以及血脂紊乱致远期心血管病风险增高等。因此,运动减轻体质量和改变生活方式至关重要,是减轻IR的一个重要途径;同时辅以胰岛素增敏剂降低体内的胰岛素及血糖,恢复卵巢排卵功能及增加卵巢对促排卵的敏感性,并减缓远期健康威胁。根据PCOS患者的临床和生化体征,治疗应个体化。
有据一项社区调查研究显示,中国PCOS代谢综合征的发生率:PCOS和非肥胖PCOS患者代谢综合征(ATPIII2005)发生率分别为19.1%和14.7。
非肥胖的PCOS患者:主要问题为不孕症和月经失调。对于非肥胖PCOS患者重点进行内膜保护相关的干预治疗。
与非肥胖的PCOS患者相比,肥胖的患者代谢异常比例增高(代谢综合征、胰岛素抵抗、高血压和高脂血症)。应重点加强体重和代谢问题上的管理,恢复卵巢排卵功能及增加卵巢对促排卵的敏感性,并减缓远期健康威胁。
多囊卵巢综合征(PCOS)病因及发病机制
人体疾病往往是基因与环境的共同作用导致疾病的发生,基因受遗传因素的影响很大,作为功能医学医生来说,会更多的关注环境因素的影响包括——图片。
>遗传学与环境的复杂相互作用(表观遗传学)
研究显示暴露于宫内高雄激素环境的雌性动物容易发生不排卵、多囊卵巢;PCOS女性携带CYP11A基因,和胰岛素改变串联重复序列,易触发雄激素和胰岛素的正常升高。
> 荷尔蒙紊乱
√ 压力与肾上腺失衡
√ PCOS是下丘脑-垂体-卵巢轴失衡
√ 甲状腺功能减退症是原因之一
一项对十几岁少女与PCOS研究表明:当甲减治疗后,超声发现卵巢囊肿好转,且LH水平也有下降。另一项发现∶PCOS患者中27%有甲状腺抗体升高;42%甲状腺超声检查与自身免疫性甲状腺炎是一致的;PCOS患者发生自身免疫性甲状腺炎的患病率比没有PCOS患者高3倍以上。
> 接触内分泌干扰物及某些药物:如抗癫痫药(AEDs)及肝酶诱导剂(苯妥英钠、苯巴比妥与卡马西平)
1.有研究曾指出,双酚A、塑化剂、防腐剂等有类雌激素作用,能与雌激素受体结合,干扰内分泌系统正常运作,导致无排卵或刺激胰岛素抵抗的发生和高雄激素血症。
2.研究表明,服用抗癫痫药物(AEDs)的时间越久,癫痫患者患PCOS的可能性越大。癫痫妇女是易罹患PCOS的特殊亚群。在这个亚群中,PCOs发生率约为26%。
> 子宫内启动氧化应激:
-
PCOS体型瘦的女性与正常肥胖女性相比,氧化应激程度更高:多囊卵巢综合症增加氧化应激,与肥胖和胰岛素抵抗无关。
-
促进动脉粥样硬化各阶段进展。
-
髓过氧化物酶(MPO)产生活性氧,可直接导致氧化应激增加和慢性炎症。
-
与空腹胰岛素、胰岛素抵抗、体重指数、甘油三酯水平和空腹血糖相关的hs-CRP阳性,与SHBG呈负相关。
> 肠道炎症和系统炎症、肠道菌群
炎症是多囊卵巢综合征的驱动力
-
PCOS患者血清MCP-1水平均明显升高。
-
PCOS患者血清C反应蛋白(CRP)水平升高。
-
血清IL-18、IL-1β、IL1-α、US-CRP明显升高。
-
PCOS患者血清中白介素18水平显著上升,并与肥胖、胰岛素抵抗、睾酮含量、LH/FSH值显著正相关。
-
PCOS患者单核巨噬细胞中MCP-1mRNA表达明显升高,引起内皮细胞功能紊乱,可能增加动脉粥样硬化发生风险。
(肠道菌群在PCOS发病中的作用及机制见图1)
肠道微生物群失调
-
水肿导致粘膜通透性变差。
-
脂多糖通过结肠阴性菌进入系统循环。
-
通过释放炎性细胞因子激活免疫系统会干扰胰岛素受体功能,增加卵巢雄激素生成,并改变正常的卵泡发育。
> 胎儿子宫内的产前畸形
以上是PCOS的病因及发病机制,那么临床一般会做哪些检查呢?
-
性激素6项
-
卵巢储备功能(AMH)
-
卵巢超声
-
皮质醇、游离睾酮
-
糖化血红蛋白
-
糖耐量及胰岛素释放
-
甲状腺功能
-
肝肾功及血脂
-
心电图
-
同型半胱氨酸(HCY)
多囊卵巢综合征发病机制总结见图1
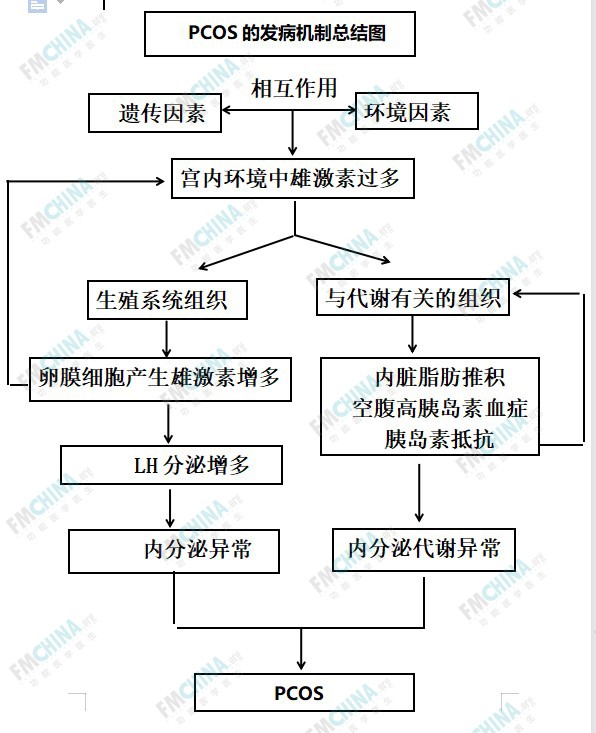
图1
PCOS生理生化指标失衡总结
> 雄激素升高∶ 睾酮水平,以及其他雄激素如雄烯二酮升高
> 胰岛素水平升高,有胰岛素抵抗
> LH/FSH比值升高(LH/FSH比值大于2,LH升高及FSH降低)
> DHEA水平升高
> 高雌酮(E1比E2高)
> 血脂异常
> 高血压
> 高同型半胱氨酸(HCY)血症
HCY 是蛋氨酸和半胱氨酸代谢过程中的中间产物,正常人体内 Hcy 的合成和分解保持平衡,其代谢过程中任何关键酶或辅助因子缺乏或酶活性降低均可导致 Hcy 代谢障碍,使之蓄积而形成高 Hcy 血症。研究结果显示提示 PCOS患者血浆Hcy 浓度升高并非叶酸、B族维生素缺乏所致,而主要与 PCOS的异常内分泌特征有关,IR可能是其血浆Hcy升高的重要原因。
多囊卵巢综合征(PCOS)案例
患者基本信息
陈女士 26岁 未婚 汉族 身高:159cm 体重:39kg BMI:15.4
BP:105/78mmHg 职业:客服人员
主诉:反复心悸、胸闷、双手抖6月余,加重伴左胸痛2小时。
现病史:患者6月前无明显诱因心悸、胸闷,双手发抖,2小时前症状加重,伴左胸痛,自感发热,无头痛,无出汗、无憋气,无咳嗽咳痰。询问病史,因工作繁忙,出现症状以来,未就诊明确原因;平素工作压力较大,经常早夜班(晚上10:00左右下班,到家11:00左右,凌晨1:00左右睡觉),睡眠障碍(入睡困难,眠浅易醒),早上7:00左右起床,晨起疲乏。未处理遂就诊。病程中精神欠佳,食欲较差,易便秘(3—4天一次,大便干结)。每周3次游泳,每次1小时,运动后有心悸症状。
个人史及既往史:小时候有过敏性紫癜发作史,治疗近2年(记不住发作年龄);2年前因月经不调在外院诊断“多囊“未予干预;年初查出FT4升高,诊断甲亢未干预;4个月前在某专科医院胃肠镜检查:糜烂性胃炎、食管白斑、结肠微腺管瘤,幽门螺杆菌感染,予抗幽门螺杆菌治疗后症状未改善,于2月前在*区人民医院复查胃镜显示:胃息肉,予以息肉摘除;因心悸、手抖查甲功:游离甲状腺素测定(FT4):23.50pmol/L↑(12.00-22.00)异常,余项未见明显异常。转入某三甲医院住院进一步检查治疗,医院进行汉密尔顿焦虑量表(HAMA)测试,得分19分,诊断肯定有焦虑;IIAMD结果18分,可能有抑郁。医院予以对症处理,医生建议抗焦虑治疗,患者因感觉治疗一周,心悸、手抖,失眠、疲乏无明显改善故未接受抗焦虑治疗及其他治疗而出院。
家族史:父母较健康,无明显特殊。月经不规律,周期2—3月/次不等,量少,痛经严重,经期心悸、胸闷、双手抖症状加重。每周3次游泳,每次1个小时。
体格检查:体型消瘦,面色微黄,毛孔粗大,额头、后背、前胸痤疮明显。舌苔薄白,甲状腺未触及肿大,乳腺未触及包块,左侧第三肋间压痛,双肺呼吸音清,两肺未闻及干湿性啰音,心尖波动位置正常,心率80次/分,律齐,各瓣膜区未闻及病理性杂音,腹部平坦,腹部无压痛、反跳痛及腹肌紧张。
临床检查结果汇总见下图
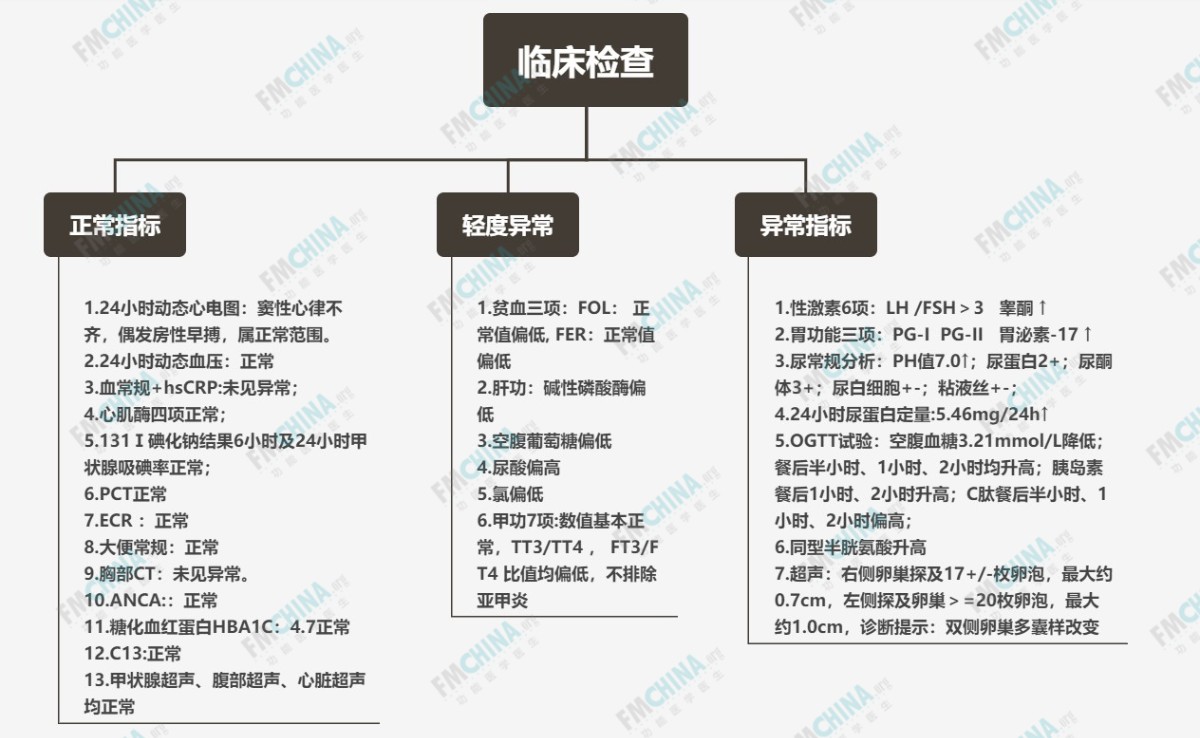
图2
MSQ医学症状问卷评分:症状评分78分,症状顺位前三位依次是:消化道;心神;能量/活动。
抑郁焦虑量表评分:总D的分数2分,总A分数12分,属于中度焦虑。
胃酸分泌功能评估:评分40分,属于胃酸缺乏。
综合评估:胃肠道慢性炎症、氧化应激、营养不良、压力失衡、代谢紊乱,毒素问题。
功能医学检测:
-
慢性食物敏感;
-
全套有机酸;
-
维生素D全套;
-
肾上腺皮质压力分析;
-
环境荷尔蒙分析;
-
睡眠激素平衡分析。
按照功能医学思维模式“两个核心问题”“五个引起疾病的环境因素”、“七个生理失衡”,我们要把损害患者健康的因素祛除,把保护患者的因素加强。
生活方式管理是重中之重——生活方式干预是PCOS患者首选的基础治疗。
国内外研究表明,影响PCOS患者生活方式改善的自身因素包括患者对疾病认知程度、自身毅力、内在动机、心理状态、BMI、受教育程度等。
第一步,加强患者自身管理,提高患者的疾病认知水平。宣教多囊知识,科普各种饮食、运动方法及行为习惯,引导其有意识地对自身疾病进行健康管理,促进其长期自觉保持健康生活方式。
第二步,依据患者工作性质等制定个性化运动方案。要求患者增加户外活动阳光有助维生素 D 的合成,适度运动可以增加胰岛素敏感性。
患者属于消瘦型多囊,每周3次1个小时的游泳超出其身体可承受的能力,机体处于过度氧化应激和压力的过度反应状态。建议建议其以舒缓的运动,比如冥想、八段锦、轻柔瑜伽为主,每周3—5次,每次30分钟以内。以身体舒适为主。
第三步 ,由医师、营养师、健康管理师等组成体重管理协作团队,共同参与患者的体重管理。围绕如何增加患者体重,营养师制定了专属餐单,指导患者养成健康的饮食习惯。减少碳水化合物摄入(减轻胰岛素抵抗),停食慢性过敏食物(减轻炎症),增加新鲜蔬菜水果(增加抗氧化维生素摄入)等。

图3
第四步,指导冥想减压放松。减少压力导致肾上腺失衡;早睡早起保证睡眠,通过睡眠修复受损细胞。同时为了平衡肾上腺功能:应用南非醉茄、磷脂酰丝氨酸,双向调节肾上腺功能。
肠道5R干预
-
移除:移除敏感食物,遵循低碳水饮食,尝试短期生酮饮食,同时给予植物抗菌剂,先后给予如G.I. Detox,Biocidin®Capsule;Olivirex®、Biocidin®Liquid等
-
替代:补充不足或缺乏的营养物质:如胃酸替代物、B族维生素、维生素D;
-
再接种:补充好的胃肠菌群(4R益生菌及广谱益生菌)来获得更为理想的平衡肠道环境;
-
修复:对胃肠黏膜的愈合和再生提供营养支持:如UltraGI Replenish;同时注意肝脏代谢的支持;
-
再平衡:恢复病人健康平衡生活方式和生理功能平衡。调整规律生活和放松瑜伽训练心理治疗。
第一个月:
在坚持5R干预的同时,还补充维生素D3、复合维生素 B族等细胞线粒体代谢所需要原料,促进细胞碳水化合物代谢,减轻胰岛素抵抗。其中复合 B 族应用含有甲基化叶酸和甲基化 B12 的活性物质,可以加速压力激素和雄激素等代谢。Ashwagandha(南非醉茄)PS 100(磷脂酰丝氨酸)联合用于焦虑及皮质醇水平比较高的症状。第一个月结束后患者症状改善不明显,第二个月加强肠道免疫,增加DHEA,支持雌激素生成;第二个月结束后患者症状改善明显,第三个月着重平衡压力和改善睡眠,抗氧化应激,加了甘氨酸螯合镁、Adreset(平衡压力)。
调理三个月患者后各项生理指标变化的对比:
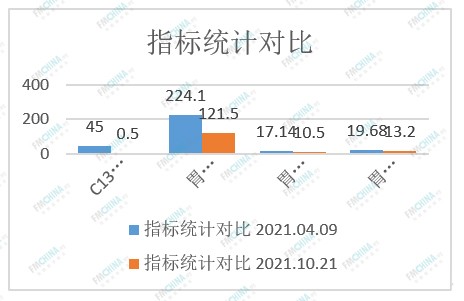
图4
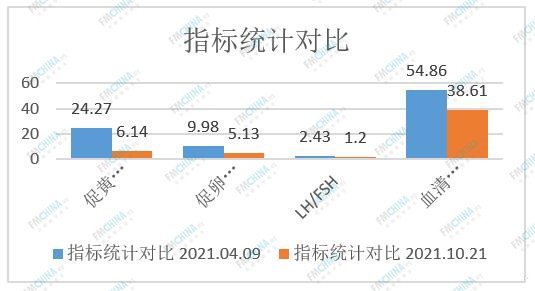
图5
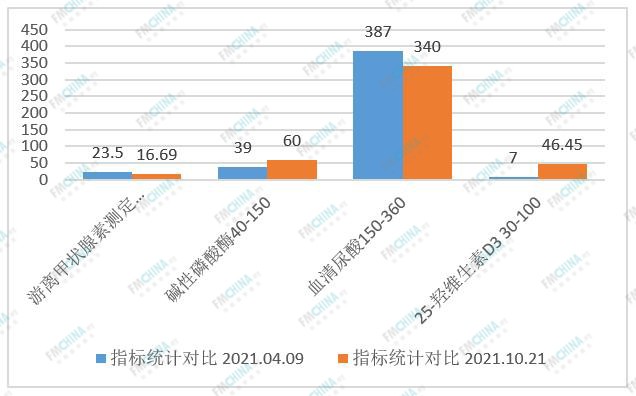
图6
超声复查:卵巢多囊样改变恢复正常
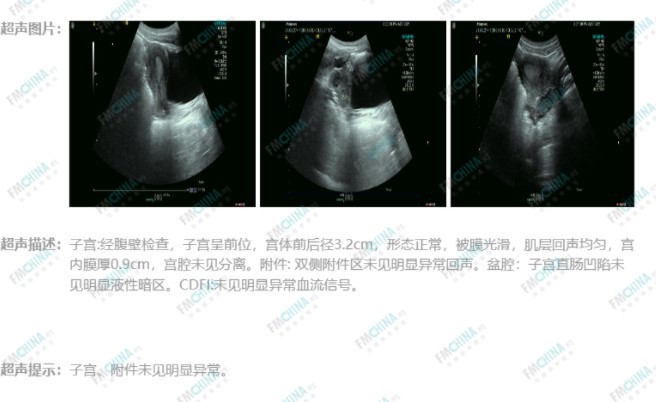
图7
患者调理前后主观感受
患者主观感受明显改善,心悸不适、手抖症状明显缓解,失眠、疲乏症状改善;焦虑、嗳气、打嗝、腹胀等症状消失;大便正常,月经周期正常,痛经明显缓解,营养状况改善,体重增加。由于考虑到费用负担,患者目前主要进行生活方式的管理。截止发稿前复查,胃功能正常、尿酸、尿常规复查均正常。但是发现患者面部仍有散在痤疮,嘱其一定要注意生活方式的管理。必要时建议做环境荷尔蒙、重金属的评估及干预。
总结:用功能医学的思维模式干预非肥胖型多囊卵巢综合征,并没有采用传统二甲双胍治疗胰岛素抵抗,而是根据患者个性化的评估后,应用细胞和组织需要的营养成份进行修复,重塑生理系统的失衡。干预原则符合功能医学"两个核心"一祛除危害健康的致病因素,如祛除不该吃的食物、不该升高的胰岛素、雄激素等等;补充维护健康所需要,而身体又缺乏的成份,如维生素 D3、细胞线粒体产生能量所需要复合B族、益生菌等等。最终达到非肥胖PCOS患者治疗应着重调整HPO轴的功能,恢复正常月经、有生育需求者帮助促排卵指导受孕的目的。
讲师简介


学习目录
学员评价

鲍勃米勒医生项目视频
0.00

NGRI功能基因组学认证课程丨模块3丨一氧化氮和NOS解偶联
0.00

NGRI功能基因组学认证课程丨模块2丨铁与芬顿反应
0.00

全民健康管理(北京)大会| 第十二届301论健
0.00

全民健康管理(北京)大会| 第十二届301论健
0.00

测试直播课程
0.00


